中考化学难题精选答案
在托盘天平两边各放一只等质量的烧杯,在两只烧杯里分别加入50g溶质质量分数为7.3%的稀盐酸,将天平调节至平衡;然后向左右两烧杯中分别加入一定质量的下列各组物质,充分反应后,天平发生偏转的是
A.1.8g铝粉和1.8g 铁粉 B.4.2g碳酸镁和2g硝酸银
C.5.6g铁粉和5.6g 锌粉 D.10g碳酸钙和5.6g氧化钙
在20℃时,把甲、乙各10g固体分别加入到两个盛有50g水的烧杯中,充分搅拌,所得甲溶液为24溶液(填饱和或不饱和);若将温度都升高到30℃,甲溶液中溶质的质量分数25 乙溶液中溶质的质量分数(填大于、等于或小于)。
24:不饱和; 25:等于
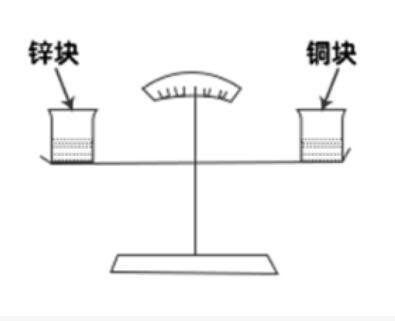
B.铜块与稀盐酸反应产生了氯化铜
C.锌块与稀盐酸反应产生了氢气
D.化学反应产生了大量水蒸气
本题考查化学反应。
第二步,根据天平的状态进行分析。
①初始:天平两端有等量稀盐酸,并处于平衡状态。
②过程:相同质量的锌块与铜块分别加入天平左右两端。
③结果:天平右侧(铜块)缓慢下降。
第三步,分析选项。
A项:天平是称质量的,整体的上升和下降只与物体的质量有关系,与体积没有关系,排除;
B项:铜块与稀盐酸不反应,排除;
C项:锌块和稀盐酸反应产生了氢气,质量变轻,符合;
D项:铜块不与稀盐酸发生反应,锌块和稀盐酸反应产生氢气,不是水蒸气,排除。
因此,选择C选项。
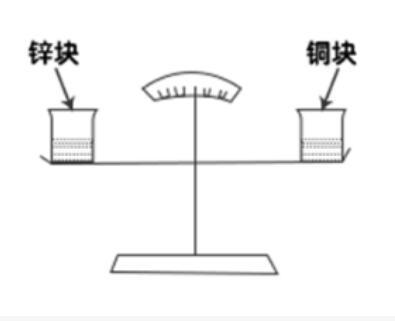
B.铜块与稀盐酸反应产生了氯化铜
C.锌块与稀盐酸反应产生了氢气
D.化学反应产生了大量水蒸气
本题考查化学反应。
第二步,根据天平的状态进行分析。
①初始:天平两端有等量稀盐酸,并处于平衡状态。
②过程:相同质量的锌块与铜块分别加入天平左右两端。
③结果:天平右侧(铜块)缓慢下降。
第三步,分析选项。
A项:天平是称质量的,整体的上升和下降只与物体的质量有关系,与体积没有关系,排除;
B项:铜块与稀盐酸不反应,排除;
C项:锌块和稀盐酸反应产生了氢气,质量变轻,符合;
D项:铜块不与稀盐酸发生反应,锌块和稀盐酸反应产生氢气,不是水蒸气,排除。
因此,选择C选项。
把30克37%的盐酸配成10%的稀盐酸时所需用的主要仪器是()。
- A、量筒、托盘天平
- B、托盘天平、烧杯、玻璃棒
- C、量筒、烧杯、玻璃棒
- D、量筒、玻璃棒
正确答案:C
此文档收集于网络,如有侵权请联系网站删除 选择题14.6%溶质质量分数为在托盘天平的两盘上各放一只等质量的烧杯,在两只烧杯里分别加入50g1、的稀盐酸,将天平调节至平衡。然后向左盘烧杯中投入一定质量的碳酸钠固体,向右盘烧杯中投入 一定质量的镁,均恰好完全反应,天平发生偏转。则下列各项操作中,能使天平重新达到平衡的是 )。( 向右盘烧杯中再加入4g稀盐酸A.将游码向右移动4.2g B. 在左盘上放7.2g碳酸钠固体C.在右盘上放4.8g镁 D的稀7.3%2、在托盘天平两边各放一只等质量的烧杯,在两只烧杯里分别加入50g溶质质量分数为盐酸,将天平调节至平衡;然后向左右两烧杯中分别加入一定质量的下列各组物质,充分反应后, 天平发生偏转的是( ) 碳酸镁和2g硝酸银 B4.2gA1.8g铝粉和1.8g 铁粉 6g氧化钙10g碳酸钙和5.6g C5.6g铁粉和5.锌粉 D、将一定量的乙醇和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未3。测得反应前后物质的质量如下表:X 知物物 质 乙醇 氧气 二氧化碳 水 X 0 反应前质量/g 4.6 8 0 0 m 5.4 4.4 0 0 反应后质量/g ) 下列判断正确的是( BX可能是该反应的催化剂 A 表中m的值为2.8 X一定含有碳元素,可能含有氢元素 D物质 C增加氧气的量可以减少X的生成 4.4 g CO2.3 g某有机物在足量的氧气中完全燃烧,生成4、常用燃烧法测定有机物的组成。现取2可能含 一定不含 O元素。对该物质的组成有下列推断:一定含和2.7 g HOC、H元素2元素的质量H、OC、 O元素 一定含O元素 分子中CH的原子个数比为2:5 分子中、 D. :8。其中正确的是 ( ) A. B. C. :比为123 的形式存在,C和,若碳元素主要以FeCFe0.245、某钢样品的含碳量为(其他杂质元素不考虑)32 (:180) )。C:(相对分子质量:CC则该钢样品中Fe和Fe的质量分数()范围是FeC124,Fe3322 C. 2.243.6 3.36 D. 2.48 A.0.032 B. 0.480.72、 CaCO6、某固体样品中除了含有在高温不分解,也不与空气成分反应的物质外,还可能含有 3经高温充分煅烧并在 gm中的一种或两种。某化学兴趣小组为探究该固体的成分,称量样品,CaO1 m至质量不再减轻为止,干燥的保护气中冷却,剩余固体的质量为 ) 。 ( 下列推断不正确的是 g。2 只供学习与交流 此文档收集于网络,如有侵权请联系网站删除 、A物质的两种溶液。下列做法不能实现MA物质的溶解度曲线。M、N两点分别表示7、右图为) ) ( N间的相互转化的是(A从溶液中析出时不带结晶水 A再降温NM:先向N中加入适量固体 A.从A N降温再加入适量固体B.从NM:先将 M降温再将其升温从MN:先将 C. M升温再将其蒸发掉部分水从MN:先将 D. aA+bB = cC+dD中,下列8、质量守恒定律是帮助我们认识化学反应实质的重要理论。在化学反应 )。说法正确的是( 之和b之和一定等于c与d A. 化学计量数a与2xg 的质量总和不一定是xg B反应,生成C和D B. 若取xg A和 的质量比的质量比一定等于生成物C和D和 C. 反应物AB 都是盐,则该反应一定是复分解反应若A和C D. ,若KOH 90KCO 2.38、9有一在空气中暴露过的KOH固体,经分析知其内含水7.62、32溶液中和,恰好完全反应。过量的酸再用20g10%的KOHWg将此样品加入到98g20%的稀硫酸中, )。蒸干中和后的溶液可得固体质量是( D无法计算 30.834.8g C34.8之间 A30.8g B中的一种或几种,取该、NaClNaCO、MgCO、CuSOK10、有一种不纯的CO固体,可能含有423323。下列判断正确稀盐酸中,恰好完全反应得到无色溶液,同时产生气体4.4g样品13.8g,加入100g CuSO A完全反应得到无色溶液,样品中一定没有 )。 的是 ( 4NaCl 不与盐酸反应,样品中一定没有 BNaCl 7.3% 所加稀盐酸中溶质的质量分数为 C NaCO和MgCO DNaCO和MgCO都能和盐酸反应生成气体,样品中一定有332323、在下列各图所示的实验装置气密性检查中,根据现象判断出漏气的是 ( )。 11 上液面高度不变下 移弹簧夹动,弹簧夹 两弹簧夹端液橡胶管面水柱 水平 A B C D 12、下列装置能达到对应实验目的的是( )。 只供学习与交流 此文档收集于网络,如有侵权请联系网站删除 的Al分别与足量且质量分数相等和13、如图13表示等质量的金属Mg )稀硫酸反应,下列叙述正确的是( 表示生成氢气的质量 AX表示反应所用时间,Y 表示反应所用时间 BX表示生成氢气的质量,Y 表示生成氢气的质量CX表示滴加稀硫酸的质量,Y X表示参加反应的金属的质量,Y表示生成氢气的质量D 相同的稀盐14、 将等质量的镁、铁、锌,分别放入三份溶质质量分数 据图中的信酸中,反应生成的H质量与反应时间的关系如图所示。根2 ( ) 息,作出的判断不正确的是 A图线x表示镁的反应情况 B铁消耗的稀盐酸质量最大 C镁、锌一定过量,铁可能反应完 D镁一定过量,锌、铁可能反应完 )之M分别跟稀盐酸反应制取氢气的质量(m)与所用的金属质量(、15、下图表示Fe、ZnMg、Al ( )间的关系图,其中正确的是 铁粉分别与同体积、同质量分数的稀硫酸充分反应。反应情56g27g铝粉、16、将 ) ( 所示。下列叙述与曲线图相符的是况如图5 铝粉、铁粉和硫酸均有剩余 A B铝粉、铁粉均反应完,硫酸有剩余 硫酸、铝粉均反应完,铁粉有剩余 C 硫酸、铁粉均反应完,铝粉有剩余 D )Cu(NO和、在一定质量的17AgNO的混合溶液中加入铁粉,充分反应后,下图一定不正确的是233 只供学习与交流 此文档收集于网络,如有侵权请联系网站删除 推断题;GF、1、框图中的物质为初中化学所学的物质,其中属于盐的是B、C、M、N,属于氧化物的是常用于改良酸性土壤。图中;D胃液中含有适量的A,可帮助消化;C是家庭中重要的调味品之表示物质间存在转化关系;部分反应物或生成物已表示两端的物质间能发生化学反应:“”“” 略去。 构成的。“离子”) ” 、 “(原子物质是由 (1)C选填 ” “ 或 分子 热量。“吸收”)(选填“放出”、 (2)A与镁条反应能 ; (3)写出D的俗名: 写出化学式:B N (4)写出GM的化学方程式: 、小梅同学学习了单质、氧化物、酸、碱、盐性质后,发现许多2不同类别的物质反应时能生产盐,于是她构建了下图所示的知识网络 图。铜及其化合物在工业上有重要的应用。借助网络图回答: (1)写出用酸和碱生产硫酸铜的化学方程式: 。 (2)请你把图中处补充完整,要求不能与图中已有信息重复。 。 ; 根据网络图可制备物 (3) 质。例如,某回收含铜电缆废料的工厂有下列制 铜的方案:写出下列步骤中 的化学方程式: 。 步骤: 。 : 。 V 步骤 。 上述方案中可能造成空气污染的步骤是 为人B可燃;气体G;气体、中不含由四种单质组成,已知:合金、合金3AAKCaNa 体新陈代谢的主要产物之一,请据图回答以下问题: 只供学习与交流 此文档收集于网络,如有侵权请联系网站删除 由哪些单质组成(用化学式表示) : (1)合金A 写出反应的化学2)(程方 : 式 ; )写出反应的化学方程式:(3 某无色气体中可能含有甲烷、一氧化碳、二氧化碳、氮气中的一种或几种,现将该气体依次通 4、装置内无水硫酸铜变蓝(无水硫DA装置内未见有浑浊出现;过如图所示装置,观察到: 酸铜遇水变蓝);最终收集到一定量干燥气体(假设每步反应都是完全的) 请回答下列问题: ; (1)由可知原混合气体中肯定不含 ; (2)由可知原混合气体中一定含有 ; (3)最终收集到的气体是 4)实验过程中记录的实验数据如下:则该气体的成分为: ( 、是一种氧化物,可作干燥剂。DAC三种固体含有同种金属元素,难溶于水,BB5、已知A、由两种元素组成,XF通常状况下为气体。DFE、含有同种非金属元素,E是常见的固体单质,、。它们的转化关系如下图(部分21,与另一种元素原子个数比为元素的质量分数为其中E37.5% 。产物已略去) 只供学习与交流 此文档收集于网络,如有侵权请联系网站删除 。 ;X 1()写出E、X物质的化学式:E 。)写出CA的化学方程式: _(2(填 组成的混合气体,如采用上图装置,则(3)实验室若分离由D和Fa中应盛有 。写试剂名称,下同),b中应盛有 是初中、DG6、 物质AJ有下图转化关系,反应条件均略去。A、B物质的组成元素相同,C、,其中一,
称量一定质量NaOH时,下列操作正确的是()。
- A、置于烧杯中在台秤上称量
- B、置于称量纸上于台秤上称量
- C、置于烧杯中在分析天平上称量
- D、置于称量纸上于分析天平上称量
正确答案:A
烧杯中装了100克浓度为10%的盐水,向该烧杯中加入一定量未知浓度的盐水后,烧杯中的盐水浓度变为15%,继续向烧杯中加入等量的该未知浓度的盐水后,烧杯中的盐水浓度变为17.5%。那么加入烧杯中的盐水的浓度是()(假设烧杯中盐水不会溢出)
- A、20%
- B、25%
- C、30%
- D、32%
正确答案:B
在天平的两托盘的烧杯中分别放入相同质量且足量的稀硫酸,调节天平平衡,再往两烧杯中分别加入等质量的Mg和Zn待烧杯中的Mg和Zn全部反应完毕后,天平的指针()。
- A、仍然留在原来的位置
- B、不能停止
- C、偏向Zn的一边
- D、偏向Mg的一边
正确答案:C
在测量盐水密度的实验步骤中,下列步骤中不必要的是()
- A、用天平测出烧杯的质量m1
- B、往烧杯内倒入适量的盐水,用天平测出烧杯和盐水的总质量m1
- C、用量筒测出烧杯中液体的体积V
- D、用天平测出倒掉盐水后空烧杯的质量m2
正确答案:A
在一定温度下,向盛有氯化钠饱和溶液的烧杯中加入氯化钠晶体后,则()
- A、晶体质量减少
- B、晶体质量不变
- C、溶质质量分数增大
- D、氯化钠溶解度增大
正确答案:B
相关考题:
- 判断题在交易发生后,如果要修改取单行,则修改前已经发生的业务仍按原取单行处理,修改后新发生的业务按照新的取单行处理。()A对B错
- 公司的组织结构可以体现出公司文化中权利距离的大小。
- 多选题关于双向宝产品的描述正确的是()A双向宝产品包括“双向外汇宝”和“双向黄金宝”B双向宝交易的前提是客户已在柜台签约双向宝交易,并开立保证金专户C双向宝交易的前提是客户网银关联账户中存在BANCS行主账户为活一本的借记卡D一张借记卡仅能签约一个人民币保证金专户和一个美元保证金专户
- 把企业看作自然的产物,属于持哪种文化态度的人:()A、内向型文化B、外向型文化C、泛指性文化D、特指性文化
- 夏多布里昂最主要的两部作品是()
- 内啮合圆柱齿轮传动,两齿轮的转向相反。
- 单选题个人网银客户查询关联账户清单交易具有三个子交易,即“()”。仅查询关联账户清单时,不打印交易凭证,无需取得客户签字回执。A1-打印当日未打印关联账户、2-查询、3-打印全部关联账户B1-打印当日交易账户、2-打印全部关联账户、3-查询C1-查询、2-打印全部关联账户、3-打印当日未打印关联账户D1-查询、2-打印当日未打印关联账户,3-打印全部关联账户
- ()是拜伦著名的浪漫主义长诗。
- 推土机推土刀架可调节成斜铲,主要用于将土壤推向一侧的工况。()
- 对中立文化和情感文化的理解不正确的是:()A、中立文化中冷静和自控能力很强B、情感文化中崇尚热情而有生命力的表达方式C、中立文化中总以一种语调来叙述事情D、情感文化中可能会偶尔通过面部表情表达他们的紧张
- 2019年3月全国教资统考初中语文学科知识与能力试题答案-
- 精编国家开放大学高级财务会计期末考试_最新国家开放大学电大《高级财务会计(本)》形考任务1-2试题及答案_
- 精编国开(中央电大)行管本科《公共政策概论》多项选择题库(珍藏版)-政策科学一词是由_
- 精编国开(中央电大)行管本科《西方行政学说》十年期末考试简答题题库-_
- 精编国开电大行管本科《城市管理学》十年期末考试选择题题库 城市管理形考作业_
- 精编经济法学期末论述题 最新国家开放大学电大专科《经济法学》论述题题库及答案(试卷号:2096)_
- 再谈宜昌市语文开卷考试_
- 《尘世小暖》阅读附答案-
- 统编版四年级下册语文期中检测卷(含答案)--
- 学霸密码:洞悉考试的底层逻辑