中考化学难题精选+答案.doc
在托盘天平两边各放一只等质量的烧杯,在两只烧杯里分别加入50g溶质质量分数为7.3%的稀盐酸,将天平调节至平衡;然后向左右两烧杯中分别加入一定质量的下列各组物质,充分反应后,天平发生偏转的是
A.1.8g铝粉和1.8g 铁粉 B.4.2g碳酸镁和2g硝酸银
C.5.6g铁粉和5.6g 锌粉 D.10g碳酸钙和5.6g氧化钙
在20℃时,把甲、乙各10g固体分别加入到两个盛有50g水的烧杯中,充分搅拌,所得甲溶液为24溶液(填饱和或不饱和);若将温度都升高到30℃,甲溶液中溶质的质量分数25 乙溶液中溶质的质量分数(填大于、等于或小于)。
24:不饱和; 25:等于
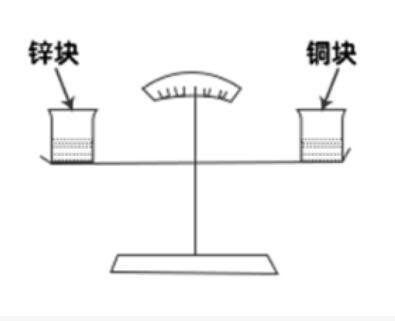
B.铜块与稀盐酸反应产生了氯化铜
C.锌块与稀盐酸反应产生了氢气
D.化学反应产生了大量水蒸气
本题考查化学反应。
第二步,根据天平的状态进行分析。
①初始:天平两端有等量稀盐酸,并处于平衡状态。
②过程:相同质量的锌块与铜块分别加入天平左右两端。
③结果:天平右侧(铜块)缓慢下降。
第三步,分析选项。
A项:天平是称质量的,整体的上升和下降只与物体的质量有关系,与体积没有关系,排除;
B项:铜块与稀盐酸不反应,排除;
C项:锌块和稀盐酸反应产生了氢气,质量变轻,符合;
D项:铜块不与稀盐酸发生反应,锌块和稀盐酸反应产生氢气,不是水蒸气,排除。
因此,选择C选项。
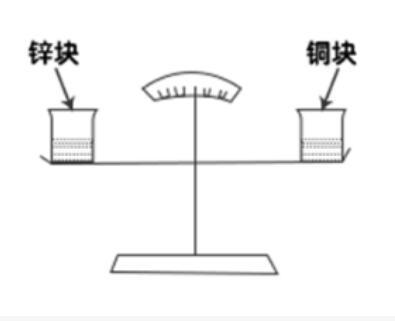
B.铜块与稀盐酸反应产生了氯化铜
C.锌块与稀盐酸反应产生了氢气
D.化学反应产生了大量水蒸气
本题考查化学反应。
第二步,根据天平的状态进行分析。
①初始:天平两端有等量稀盐酸,并处于平衡状态。
②过程:相同质量的锌块与铜块分别加入天平左右两端。
③结果:天平右侧(铜块)缓慢下降。
第三步,分析选项。
A项:天平是称质量的,整体的上升和下降只与物体的质量有关系,与体积没有关系,排除;
B项:铜块与稀盐酸不反应,排除;
C项:锌块和稀盐酸反应产生了氢气,质量变轻,符合;
D项:铜块不与稀盐酸发生反应,锌块和稀盐酸反应产生氢气,不是水蒸气,排除。
因此,选择C选项。
把30克37%的盐酸配成10%的稀盐酸时所需用的主要仪器是()。
- A、量筒、托盘天平
- B、托盘天平、烧杯、玻璃棒
- C、量筒、烧杯、玻璃棒
- D、量筒、玻璃棒
正确答案:C
选择题1、在托盘天平的两盘上各放一只等质量的烧杯,在两只烧杯里分别加入50g溶质质量分数为14.6%的稀盐酸,将天平调节至平衡。然后向左盘烧杯中投入一定质量的碳酸钠固体,向右盘烧杯中投入一定质量的镁,均恰好完全反应,天平发生偏转。则下列各项操作中,能使天平重新达到平衡的是 ( )。A.将游码向右移动4.2g B.向右盘烧杯中再加入4g稀盐酸C.在右盘上放4.8g镁 D在左盘上放7.2g碳酸钠固体2、(2009青岛)在托盘天平两边各放一只等质量的烧杯,在两只烧杯里分别加入50g溶质质量分数为7.3%的稀盐酸,将天平调节至平衡;然后向左右两烧杯中分别加入一定质量的下列各组物质,充分反应后,天平发生偏转的是( )A1.8g铝粉和1.8g 铁粉 B4.2g碳酸镁和2g硝酸银C5.6g铁粉和5.6g 锌粉 D10g碳酸钙和5.6g氧化钙3、将一定量的乙醇和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未知物X。测得反应前后物质的质量如下表:物质乙醇氧气二氧化碳水X反应前质量/g4.68000反应后质量/g004.45.4m下列判断正确的是( ) A表中m的值为2.8 BX可能是该反应的催化剂 C增加氧气的量可以减少X的生成 D物质X一定含有碳元素,可能含有氢元素4、 常用燃烧法测定有机物的组成。现取2.3 g某有机物在足量的氧气中完全燃烧,生成4.4 g CO2和2.7 g H2O。对该物质的组成有下列推断:一定含C、H元素 一定不含O元素 可能含O元素 一定含O元素 分子中C、H的原子个数比为2:5 分子中C、H、O元素的质量比为12:3:8。其中正确的是( ) A. B. C. D.5、某钢样品的含碳量为0.24(其他杂质元素不考虑),若碳元素主要以Fe2C和Fe3C的形式存在,则该钢样品中Fe2C和Fe3C的质量分数()范围是(相对分子质量:Fe2C:124,Fe3C:180)( )。 A.0.032 B. 0.480.72 C. 2.243.36 D. 2.483.66、某固体样品中除了含有在高温不分解,也不与空气成分反应的物质外,还可能含有 CaCO3 、CaO中的一种或两种。某化学兴趣小组为探究该固体的成分,称量样品m1 g,经高温充分煅烧并在干燥的保护气中冷却,至质量不再减轻为止,剩余固体的质量为m2 g。下列推断不正确的是( )。 7、右图为A物质的溶解度曲线。M、N两点分别表示A物质的两种溶液。下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水) ( ) A.从NM:先向N中加入适量固体A再降温 B.从NM:先将N降温再加入适量固体A C.从MN:先将M降温再将其升温 D.从MN:先将M升温再将其蒸发掉部分水8、质量守恒定律是帮助我们认识化学反应实质的重要理论。在化学反应aA+bB = cC+dD中,下列 说法正确的是( )。 A. 化学计量数a与b之和一定等于c与d之和 B. 若取xg A和xg B反应,生成C和D的质量总和不一定是2xg C. 反应物A和B的质量比一定等于生成物C和D的质量比 D. 若A和C都是盐,则该反应一定是复分解反应9有一在空气中暴露过的KOH固体,经分析知其内含水7.62、K2CO3 2.38、KOH 90,若将此样品Wg加入到98g20%的稀硫酸中,过量的酸再用20g10%的KOH溶液中和,恰好完全反应。蒸干中和后的溶液可得固体质量是( )。 A30.8g B34.8g C30.834.8之间 D无法计算10、有一种不纯的K2CO3固体,可能含有Na2CO3、MgCO3、CuSO4、NaCl中的一种或几种,取该样品13.8g,加入100g稀盐酸中,恰好完全反应得到无色溶液,同时产生气体4.4g。下列判断正确的是 ( )。 A完全反应得到无色溶液,样品中一定没有CuSO4 BNaCl不与盐酸反应,样品中一定没有NaCl C所加稀盐酸中溶质的质量分数为7.3% DNa2CO3和MgCO3都能和盐酸反应生成气体,样品中一定有Na2CO3和MgCO311、在下列各图所示的实验装置气密性检查中,根据现象判断出漏气的是 ( )。 A B C D 12、 下列装置能达到对应实验目的的是( )。 13、如图13表示等质量的金属Mg和Al分别与足量且质量分数相等的稀硫酸反应,下列叙述正确的是( ) AX表示反应所用时间,Y表示生成氢气的质量 BX表示生成氢气的质量,Y表示反应所用时间 CX表示滴加稀硫酸的质量,Y表示生成氢气的质量 DX表示参加反应的金属的质量,Y表示生成氢气的质量14、 将等质量的镁、铁、锌,分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2质量与反应时间的关系如图所示。根据图中的信息,作出的判断不正确的是 ( ) A图线x表示镁的反应情况 B铁消耗的稀盐酸质量最大 C镁、锌一定过量,铁可能反应完 D镁一定过量,锌、铁可能反应完15、下图表示Fe、Zn、Mg、Al分别跟稀盐酸反应制取氢气的质量(m)与所用的金属质量(M)之间的关系图,其中正确的是 ( ) 16、将27g铝粉、56g铁粉分别与同体积、同质量分数的稀硫酸充分反应。反应情况如图5所示。下列叙述与曲线图相符的是 ( ) A铝粉、铁粉和硫酸均有剩余 B铝粉、铁粉均反应完,硫酸有剩余 C硫酸、铝粉均反应完,铁粉有剩余 D硫酸、铁粉均反应完,铝粉有剩余 17、在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,下图一定不正确的是 推断题1、框图中的物质为初中化学所学的物质,其中属于盐的是B、C、M、N,属于氧化物的是F、G;胃液中含有适量的A,可帮助消化;C是家庭中重要的调味品之;D常用于改良酸性土壤。图中“”表示两端的物质间能发生化学反应:“”表示物质间存在转化关系;部分反应物或生成物已略去。 (1)C物质是由 (选填“分子”、“原子”或 “离子”)构成的。 (2)A与镁条反应能 (选填“放出”、“吸收”)热量。 (3)写出D的俗名: ; 写出化学式:B N (4)写出GM的化学方程式: 2、小梅同学学习了单质、氧化物、酸、碱、盐性质后,发现许多不同类别的物质反应时能生产盐,于是她构建了下图所示的知识网络图。铜及其化合物在工业上有重要的应用。借助网络图回答: (1)写出用酸和碱生产硫酸铜的化学方程式: 。 (2)请你把图中处补充完整,要求不能与图中已有信息重复。 ; 。 (3)根据网络图可制备物质。例如,某回收含铜电缆废料的工厂有下列制铜的方案: 写出下列步骤中的化学方程式: 步骤: 。 步骤V: 。 。 上述方案中可能造成空气污染的步骤是 。 3、 合金A由四种单质组成,已知:合金A中不含K、Ca、Na;气体B可燃;气体G为人体新陈代谢的主要产物之一,请据图回答以下问题:(1)合金A由哪些单质组成(用化学式表示): (2)写出反应的化学方程式: ;(3)写出反应的化学方程式: 4、 某无色气体中可能含有甲烷、一氧化碳、二氧化碳、氮气中的一种或几种,现将该气体依次通过如图所示装置,观察到:A装置内未见有浑浊出现;D装置内无水硫酸铜变蓝(无水硫酸铜遇水变蓝);最终收集到一定量干燥气体(假设每步反应都是完全的)请回答下列问题:(1) 由可知原混合气体中肯定不含 ;(2)由可知原混合气体中一定含有 ;(3)最终收集到的气体是 ;(4)实验过程中记录的实验数据如下:则该气体的成分为: 5、 已知A、B、C三种固体含有同种金属元素,A难溶于水,B是一种氧化物,可作干燥剂。D、E、F含有同种非金属元素,E是常见的固体单质,D、F通常状况下为气体。X由两种元素组成,其中E元素的质量分数为37.5%,与另一种元素原子个数比为21。它们的转化关系如下图(部分产物已略去)。 (1)写出E、X物质的化学式:E ; X 。(2)写出CA的化学方程式: _。(3)实验室若分离由D和F组成的混合气体,如采用上图装置,则a中应盛有 (填写试剂名称,下同),b中应盛有 。6、 物质AJ有下图转化关系,反应条件均略去。A、B物质的组成元素相同,C、D、G是初中化学中常见的单质,I是金属。H的相对分子质量为100,组成元素的原子个数比为3:2,其中一种元素的质量分数为28%。 试回答:上述转化中属于分解反应的是 (填序号);A、J、H的化学式为A 、J 、H ;
称量一定质量NaOH时,下列操作正确的是()。
- A、置于烧杯中在台秤上称量
- B、置于称量纸上于台秤上称量
- C、置于烧杯中在分析天平上称量
- D、置于称量纸上于分析天平上称量
正确答案:A
某学生在用托盘天平测物体质量时,已将天平调好,估计物体质量约20g,将物体和砝码分别放入左右盘中后,发现指针偏向左侧,他应该()。
- A、减少砝码
- B、增加砝码
- C、向左移横梁右端的平衡螺母
- D、向右移横梁右端的平衡螺母
正确答案:B
某同学设计了一种实验方案: 方案:(1)用调节好的天平测出空烧杯的质量m1;(2)向烧杯中倒入一些食用油,测出它们的总质量m2,则这些食用油的质量为m2-m1;(3)再将烧杯中的食用油倒入量筒中,测出食用油的体积V;(4)计算出食用油的密度ρ。 问题: (1)指出该方案的不足之处。 (2)设计教学片段帮助学生改进实验。
正确答案: (1)第三步中,烧杯中液体会倒不干净,会有剩余,测量的质量不准,造成测量出的密度偏小。
(2)师:你的方案总体来说是可行的,但是略有瑕疵。烧杯中的液体倒不干净会怎么样?
生:所测质量会偏小,造成测量密度偏小。
师:但是用烧杯倒液体肯定倒不干净,直接测量不可行,应该怎么办?
生:对!应该采用间接测量的方法。先用天平测出装有适量食用油的烧杯的总质量m1;将烧杯中的一部分食用油倒入量筒中,记录量筒中食用油的体积V;测出烧杯及剩下食用油的总质量m2;这样就可以计算出食用油的密度ρ了。
师:嗯,不错。用这种方案,测量结果误差更小。
在天平的两托盘的烧杯中分别放入相同质量且足量的稀硫酸,调节天平平衡,再往两烧杯中分别加入等质量的Mg和Zn待烧杯中的Mg和Zn全部反应完毕后,天平的指针()。
- A、仍然留在原来的位置
- B、不能停止
- C、偏向Zn的一边
- D、偏向Mg的一边
正确答案:C
在测量盐水密度的实验步骤中,下列步骤中不必要的是()
- A、用天平测出烧杯的质量m1
- B、往烧杯内倒入适量的盐水,用天平测出烧杯和盐水的总质量m1
- C、用量筒测出烧杯中液体的体积V
- D、用天平测出倒掉盐水后空烧杯的质量m2
正确答案:A
相关考题:
- 关于人格与性格,下面说法错误的是( )A.人格比性格更多地受环境影响B.性格带有正面或负面的明显社会评价色彩C.性格是人格中涉及社会评价的那部分内容D.性格指的是人的一惯的和稳定的心理特征、思维和行为方式
- 可以自由兑换其他国家货币的外汇称为现汇.
- ( 难度:中等)Hive支持哪些压缩格式A.gzipB.mp4C.snappyD.rar
- ( 难度:中等)Hive与传统关系型数据库对比,优势有A.计算能力更强B.延迟更低C.扩展性更好D.索引各类更多
- 美国在冷战之后进行了三次大的战略调整,第一次克林顿政府提出了什么?下列选项错误的是A.“全球反恐战争B.“亚太再平衡C.“称霸战争D.“参与和扩展战略
- 如“清算资金往来——同城票据清算"科目余额为借方,则表示本行本次交换为应收差额。
- 最底层的需要是( )。A.生理需要B.安全需要C.归属和爱的需要D.尊重的需要
- 信息化战争的本质,仍然是政治的继续,是流血的政治,是文明的战争。
- ( 难度:中等)hive基本表类型有哪些A.内部表B.外部表C.分区表D.桶表
- 下面哪个概念不属于社会学习理论( )。A.观察学习B.自我效能C.自我实现D.替代学习