新药进行临床试验必须提供A.系统药理研究数据B.急慢性毒性观察结果C.新药作用谱D.LDE.临床前研究资料
新药进行临床试验必须提供
A.系统药理研究数据
B.急慢性毒性观察结果
C.新药作用谱
D.LD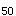
E.临床前研究资料
B.急慢性毒性观察结果
C.新药作用谱
D.LD
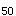
E.临床前研究资料
参考解析
解析:
相关考题:
新药临床试验应遵循四个必须,其中包括A.必须有国务院的批准B.必须遵守赫尔辛基宣言S 新药临床试验应遵循四个必须,其中包括A.必须有国务院的批准B.必须遵守赫尔辛基宣言C.必须符合GCPD.必须在中检所进行试验E.必须符合GMP
临床试验分为I、Ⅱ、Ⅲ、Ⅳ期。申请新药注册时( )。A.必须进行I、Ⅱ、Ⅲ、Ⅳ期临床实验B.可以只进行I、Ⅱ期临床实验C.可以只进行Ⅱ、Ⅲ期临床试验D.可以只进行Ⅲ、Ⅳ期临床试验E.可以只进行Ⅱ、Ⅳ期临床试验
临床试验分为I、Ⅱ、Ⅲ、Ⅳ期,申请新药注册时A.必须进行I、Ⅱ、Ⅲ、Ⅳ期临床试验B.可以只进行I、Ⅱ期临床试验C.可以只进行Ⅱ、Ⅲ期临床试验D.可以只进行Ⅲ、Ⅳ期临床试验E.可以只进行Ⅱ、Ⅳ期临床试验
目的是观察人体对于新药的耐受程度和药代动力学。为制定给药方案提供依据的是A.I期临床试验SXB 目的是观察人体对于新药的耐受程度和药代动力学。为制定给药方案提供依据的是A.I期临床试验B.Ⅱ期临床试验C.Ⅲ期临床试验D.Ⅳ期临床试验E.生物等效性试验
新药申请注册程序的主要步骤是A.新药非临床试验申请、新药临床试验申请B.新药非临床试验申请、新药生产申请C.新药非临床试验申请、新药临床试验申请、新药生产申请D.新药生产申请E.新药临床试验申请、新药生产申请
新药临床评价的分期,新药获得批准试生产后进行的扩大化临床试验阶段,进一步验证药物对目标适应证患者的治疗作用和安全性,评价利益和风险关系,最终为药物注册申请获得批准提供充分的依据,属于A.Ⅰ期临床试验B.Ⅱ期临床试验C.Ⅲ期临床试验D.Ⅳ期临床试验E.Ⅴ期临床试验
以下关于药物临床研究的说法正确的是A.临床研究包括临床试验或生物等效性试验B.申请新药注册应进行临床试验或生物等效性试验C.临床试验分四期D.申请新药可进行Ⅰ、Ⅱ、Ⅲ期临床试验,有时可进行Ⅱ、Ⅲ期或Ⅲ期临床试验
关于药物的临床试验叙述正确的是A.须经国家药监局批准,必须执行《药物临床试验质量管理规范》B.临床试验分为Ⅰ、Ⅱ、Ⅲ、Ⅳ期C.新药在批准上市前,应当进行Ⅰ、Ⅱ、Ⅲ期临床试验D.Ⅲ期为治疗作用确证阶段
下述不正确的是()A、研究者在临床试验前必须获得药品监督管理部门批准进行临床试验的批文B、研究者在临床试验前必须获得药检部门对准备用于人体试验的该批新药的质量检验合格证明C、研究者在临床试验前必须审查全部研究资料D、研究者在临床试验前必须熟悉申办者所提供的与临床试验有关的资料与文献E、参加研究的医师不需要掌握研究计划内容与要求
新药研制单位向国家食品药品监督管理局药品评审中心进行注册申请和技术评审必须呈报的内容之一,也是新药评价的最后阶段的是:()A、新药临床前研究B、新药临床试验Ⅰ期C、新药临床试验Ⅱ期D、新药临床药理评价
新药申请注册程序的主要步骤是()A、新药非临床试验申请、新药临床试验申请B、新药非临床试验申请、新药生产申请C、新药非临床试验申请、新药临床试验申请、新药生产申请D、新药生产申请E、新药临床试验申请、新药生产申请
单选题下述不正确的是()A研究者在临床试验前必须获得药品监督管理部门批准进行临床试验的批文B研究者在临床试验前必须获得药检部门对准备用于人体试验的该批新药的质量检验合格证明C研究者在临床试验前必须审查全部研究资料D研究者在临床试验前必须熟悉申办者所提供的与临床试验有关的资料与文献E参加研究的医师不需要掌握研究计划内容与要求
多选题新药进行临床试验必须提供?()A系统药理研究数据B慢性毒性实验结果CLD50D临床前研究资料E核算药物成本