向原电池的负极中加入NaCl,则原电池电动势的变化是:A.变大B.变小C.不变D.不能确定
向原电池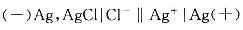 的负极中加入NaCl,则原电池电动势的变化是:
的负极中加入NaCl,则原电池电动势的变化是:
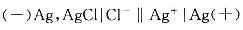 的负极中加入NaCl,则原电池电动势的变化是:
的负极中加入NaCl,则原电池电动势的变化是:
A.变大
B.变小
C.不变
D.不能确定
B.变小
C.不变
D.不能确定
参考解析
解析:提示:负极氧化反应:Ag+Cl-=AgCl+e
正极还原反应:Ag++e=Ag
电池反应为:Ag++Cl- = AgCl

由于负极中加入NaCl,Cl-浓度增加,则负极电极电势减小,正极电极电势不变,则电池的电动势增大。
正极还原反应:Ag++e=Ag
电池反应为:Ag++Cl- = AgCl

由于负极中加入NaCl,Cl-浓度增加,则负极电极电势减小,正极电极电势不变,则电池的电动势增大。
相关考题:
下列有关原电池的叙述中,正确的是( )。A: 原电池是将化学能转化为电能的装置B: 用导线连接的两种不同金属同时插入液体中.能形成原电池C: 在原电池中,电子流出的一极是负极,发生氧化反应D: 原电池放电时,电解质溶液中的阳离子向正极移动
下列关于原电池的叙述中正确的是A.原电池能将化学能转变为电能 ? ? ? ?B.原电池负极发生的是还原反应 ? ? ? ? ?C.原电池在工作时,正极不断产生电子并经外电路流向负极 ? ? ?D.原电池的电极只能由两种不同的金属构成
在300K、101.325kPa下,有一原电池的电动势E为2V,若在该温度、压力下,原电池向环境可逆输出了2F的电量,则此原电池对环境做了()的电功。A.385.94kJB.-385.94kJC.-4kJD.-192.97kJ
下列说法中错误的是()。A、原电池正极发生还原反应,负极发生氧化反应B、原电池中氧化剂在原电池的正极C、原电池的电池反应就是作为氧化剂的物质同作为还原剂的物质起反应D、原电池中,电极电位较低的电对组成电池的正极
电位分析法中,分析钾离子活度(pK值),依据的是()A、原电池电动势与K+浓度成线形关系B、原电池电动势与K+活度成线形关系C、原电池电动势与K+浓度对数成线形关系D、原电池电动势与K+活度对数成线形关系
单选题在300K、101.325kPa下,有一原电池的电动势E为2V,若在该温度、压力下,原电池向环境可逆输出了2F的电量,则此原电池对环境做了()的电功。A385.94kJB-385.94kJC-4kJD-192.97kJ
单选题电位分析法中,分析钾离子活度(pK值),依据的是()A原电池电动势与K+浓度成线形关系B原电池电动势与K+活度成线形关系C原电池电动势与K+浓度对数成线形关系D原电池电动势与K+活度对数成线形关系