向原电池(-)Ag,AgCl Cl- Ag+ Ag(+)的负极中加入NaCl,则原电池电动势的变化是:A.变大B.变小C.不变D.不能确定
向原电池(-)Ag,AgCl Cl- Ag+ Ag(+)的负极中加入NaCl,则原电池电动势的变化是:
A.变大
B.变小
C.不变
D.不能确定
B.变小
C.不变
D.不能确定
参考解析
解析:提示 负极氧化反应:Ag+Cl- =AgCl+e
正极还原反应:Ag++e=Ag
电池反应为:Ag++Cl-=AgCl
原电池负极能斯特方程式为: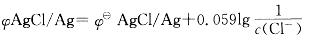
由于负极中加入NaCl,Cl-浓度增加,则负极电极电势减小,正极电极电势不变,
则电池的电动势增大。
正极还原反应:Ag++e=Ag
电池反应为:Ag++Cl-=AgCl
原电池负极能斯特方程式为:
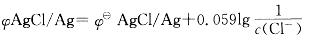
由于负极中加入NaCl,Cl-浓度增加,则负极电极电势减小,正极电极电势不变,
则电池的电动势增大。
相关考题:
已知AgCI的KSP=1.8×10-10,向AgNO3溶液中加HCl,生成AgCl沉淀。沉淀后测得溶液中c(Cl-)=0.2mol·L-1,则下述结论正确的是( )。A、残留的c(Ag+)=1.3×10-5mol·L-1B、残留的c(Ag+)=8.0×10-10mol·L-1C、溶液中Ag+沉淀完全D、溶液中Ag+未沉淀完全
在标准条件下将氧化还原反应Fe2++Ag+Fe3++Ag装配成原电池,原电池符号为()A、(-)Fe2+|Fe3+‖Ag+½Ag(+)B、(-)Ag|Ag+‖Fe3+½Fe2+(+)C、(-)Pt|Fe2+,Fe3+‖Ag+½Ag(+)D、(-)Ag|Ag+‖Fe2+,Fe3+½Pt(+)
将反应Fe2++Ag+→Fe3++Ag构成原电池,其电池符号为()。A、(-)Fe2+∣Fe3+‖Ag+∣Ag(+)B、(-)Pt∣Fe2+∣Fe3+‖Ag+∣Ag(+)C、(-)Pt∣Fe2+.Fe3+‖Ag+∣Ag(+)D、(-)Pt∣Fe2+,Fe3+‖Ag+∣Ag∣Pt(+)
下列反应中ΔrGmΘ等于产物ΔfGmΘ的是哪个?()A、Ag+(aq)+Cl-(aq)→AgCl(s)B、2Ag(s)+Cl2(g)→2AgCl(s)C、Ag(s)+1/2Cl2(g)→AgCl(s)D、Ag(s)+1/2Cl2(l)→AgCl(s)
单选题向原电池(-)Ag,AgCl|Cl-‖Ag+|Ag(+)的负极中加入NaCl,则原电池电动势的变化是( )。[2013年真题]A变大B变小C不变D不能确定