暴露在常温空气中的碳并不燃烧,只是由于反应C(s)+O2(g)=CO2(g)[已知CO2(g) C.逆反应速率大于正反应速率 D.上述原因均不正确
暴露在常温空气中的碳并不燃烧,只是由于反应C(s)+O2(g)=CO2(g)[已知CO2(g) 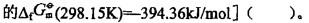

C.逆反应速率大于正反应速率 D.上述原因均不正确
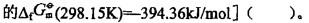

C.逆反应速率大于正反应速率 D.上述原因均不正确
参考解析
解析:提示:反应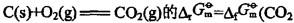 ,正向是自发的,但由于该反应速率缓慢造成在常温常压下并没有反应。
,正向是自发的,但由于该反应速率缓慢造成在常温常压下并没有反应。
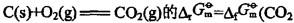 ,正向是自发的,但由于该反应速率缓慢造成在常温常压下并没有反应。
,正向是自发的,但由于该反应速率缓慢造成在常温常压下并没有反应。
相关考题:
表示CO2(g)的标准摩尔生成焓的反应是()。 ACO(g)+1/2O2(g)=CO2(g)ΔfHom=-283.0kJ/molBC(金刚石)+O2(g)=2CO2(g)ΔfHθm=-395.8kJ/molCC(石墨)+2O2(g)=2CO2(g)ΔfHθm=-787.0kJ/molDC(石墨)+O2(g)=CO2(g)ΔfHθm=-393.5kJ/mol
下列反应中表达式正确的是。A、Na(s)+1/2Cl2(g)=NaCl(s)ΔrHmθ=ΔfHmθ(NaCl,s)B、C(石墨)+H2(g)=1/2C2H4(g)ΔrHmθ=ΔfHmθ(C2H4,g)C、CO(g)+1/2O2(g)=CO2(g)ΔrHmθ=ΔfHmθ(CO2,g)D、CH3OH(g)+O2(g)=CO(g)+2H2O(g)ΔrHmθ=ΔcHmθ(CH3OH,g)
已知反应:C(石墨)+O2(g)=CO2(g)=-393.7kJ•mol-1C(金刚石)+O2(g)=CO2(g)=-395.8kJ•mol-1则反应C(石墨)C(金刚石)的等于()A、-789.5kJ•mol-1B、2.1kJ•mol-1C、-2.1kJ•mol-1D、789.5kJ•mol-1
在标准条件下,下列反应式中能表示CO2的ΔfHmθ(298.15K)的反应式为()A、C(金刚石)+ O2(g)= CO2(g)B、C(石墨)+O2(g)= CO2(g)C、CO(g)+1/2O2(g)= CO2(g)D、CO2(g)=CO(g)+1/2O2(g)
反应 CaCO3(s) → CaO(s) + CO2(g)已知: CaCO3(s) CaO(s) CO2(g) △Gθ(KJ/mol) -1128.0 -604.2 -394.4 △fHθ(KJ/mol) -1206.9 -635.1 -393.5 Sθ(J/mol/K) 92.9 39.7 213.6上述反应发生的最低温度应为多少?
碳燃烧反应为基元反应,其方程式为C(s)+O2(g)→CO2(g)则其反应速率方程式为()A、υ=kc(C)c(CO2)B、υ=kc(O2)c(CO2)C、υ=kc(CO2)D、υ=kc(O2)
已知:C(s)+O2(g)CO2(g)△H=-393.5kJ·mol-1 Mg(s)+O2(g)MgO(s)△H=-601.8kJ·mol-1 Mg(s)+C(s)+O2(g)MgCO3(s)△H=-1113kJ·mol-1 则MgO(s)+CO2(g)MgCO3(s)的△H为()kJ·mol-1A、-235.4B、-58.85C、-117.7D、-1321.3
下列反应中,反应的标准摩尔焓变等于产物的标准摩尔生成焓的是()A、CaO(s)+CO2(g)→CaCO3(s)B、1/2H2(g)+1/2Br2(g)→HBr(g)C、6Li(s)+N2(g)→2Li3N(s)D、K(s)+O2(g)→KO2(s)
反应CH2Cl2(l)+O2(g)CO2(g)+2HCl(g)在常温常压下能否自发进行?怎样判断?已知298K时△G(kJ·mol-1分别为CH2Cl2(l):-67;CO2(g):-394;HCl(g):-95
下列哪一个反应的焓变等于CO2(g)的标准摩尔生成焓:()A、CO(g)+C(s)==CO2(g)ΔrHm1B、CO(g)+1/2O2(s)==CO2(g)ΔrHm2C、O2(g)+C(s)==CO2(g)ΔrHm3D、2O2(g)+2C(s)==2CO2(g)ΔrHm4
已知反应C(s)+O2(g)=CO2(g)的标准平衡常数为K1ө,CO(g)+1/2O2(g)=CO2((g)的标准平衡常数为Kө2,2C(s)+O2(g)=2CO(g)的标准平衡常数为Kө3,则Kө3与Kө1/和Kө2的关系为()
已知1000K时, (1)CO(g)+(1/2)O2(g)=CO2(g),Kø⑴=1.659×1010 (2)C(s)+CO2(g)=2CO(g),Kø⑵=1.719 则反应C(s)+(1/2)O2(g)=CO(g)的Kø⑶为()A、9.651×1010B、1.036×1010C、4.731×1010D、2.852×1010
表示CO2生成热的反应是()A、CO(g)+1/2O2(g)=CO2(g)ΔrHmθ=-238.0kJ.mol-1B、C(金刚石)+O2(g)=CO2(g)ΔrHmθ=-395.4kJ.mol-1C、2C(金刚石)+2O2(g)=2CO2(g)ΔrHmθ=-787.0kJ.mol-1D、C(石墨)+O2(g)=CO2(g)ΔrHmθ=-393.5kJ.mol-1
在下列反应中,Qp=Qv的反应为()A、CaCO3(s)→CaO(s)+CO2(g)B、N2(g)+3H2(g)→2NH3(g)C、C(s)+O2(g)→CO2(g)D、2H2(g)+O2(g)→2H2O(l)
已知反应C(s)+O2(g)→CO2(g)的热效应ΔH,下列说法中,何者不正确?()A、ΔH是CO2(g)的生成热B、ΔH是C(s)的燃烧热C、ΔH与反应的ΔU的数值不相等D、ΔH与反应的ΔU的数值相等
1个大气压下,C(石墨)+O2(g)﹦CO2(g)的反应热为ΔrHθm,下列说明中错误的是()A、ΔrHθm就是CO2(g)的生成焓ΔfHθmB、ΔrHθm就是C(石墨)的燃烧焓C、ΔrHθm=ΔrUθmD、ΔrHθmΔrUθm
单选题下列反应中,熵增加最多的是( )。A2SO2(g)+O2(g)=2SO3(g)BNH4NO3(s)=N2O(g)+2H2O(l)CMnO2(s)+Mn(s)=2MnO(s)DCO(g)+H2O(g)=CO2(g)+H2(g)
单选题下列反应在常温下均为非自发反应,在高温下仍为非自发反应的是()。AAg2O(g)→2Ag(s)+(1/2)O2(g)BFe2O3(s)+(3/2)C(s)→2Fe+(3/2)CO2(g)CN2O4(g)→2NO2(g)D6C(s)+6H2O(l)→C6H12O6(s)
填空题下述3个反应: (1)S(s)+O2(g)→SO2(g) (2)H2(g)+O2(g)→H2O2(g) (3)C(s)+H2O(g)→CO2(g)+H2(g) 按ΔrSθm增加的顺序为()。
单选题下列反应中,ΔrSmθ最大的是()。AC(s)+O2(g)→CO2(g)B2SO2(g)+O2(g)→2SO3(g)C3H2(g)+N2(g)→2NH3(g)DCuSO4(s)+5H2O(l)→CuSO4•5H2O(s)